
- La materia está constituida por partículas muy pequeñas llamadas átomos, que son indivisibles y no se pueden destruir.
- Los átomos de un mismo elemento son iguales entre sí, tienen su propio peso y cualidades propias.
- Los átomos permanecen sin división, aún cuando se combinen en las reacciones químicas.
- Los átomos de elementos diferentes se pueden combinar en proporciones distintas y formar más de un compuesto.
MODELO ATÓMICO DE THOMSON

El modelo de Dalton era insuficiente para explicar estos fenómenos. Es por eso que en 1898, J.J Thomson propone un modelo para la distribución de los electrones en el átomo. Propuso que el átomo se componía de dos partes, una negativa y una positiva. La parte negativa estaba constituida por electrones, los cuales se encontraban según este modelo inmersos en una masa de carga
positiva a manera de pasas en un pastel. Una nube positiva que contenía las pequeñas partículas negativas (los electrones) suspendidos en ella. El número de cargas negativas era el adecuado para neutralizar la carga positiva. Si el átomo perdía un electrón, la estructura quedaría positiva; y si ganaba un electron, la carga final sería negativa. De esta forma, explicaba la formación de iones. Pero no daba explicación a otro tipo de fenómenos.
MODELO ATÓMICO DE RUTHERFORD

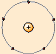
El modelo atómico de Rutherford en la comprensión de la materia. Pues introduce la idea de un núcleo central en el que se concentraría toda la carga positiva del átomo y casi toda la masa, y en torno a el y a cierta distancia se encontrarían los electrones girando alrededor del núcleo en órbitas. Estas orbitas no estaban definidas, por lo que el átomo no tendría tampoco forma ni tamaño definido.
El modelo daba explicación satisfactoria a los resultados de sus experimentos con la lámina de oro.
Sin embargo modelo tiene una dificultad proveniente de la electrodinámica clásica que predice que una partícula cargada acelerada, como sería necesario para mantenerse en órbita, emitiría radiación electromagnética, perdiendo energía. Cuando toda la energía del átomo se hubiera radiado, vendría la caída de los electrones sobre el núcleo. Se trata, por tanto de un modelo físicamente inestable,
desde el punto de vista de la física clásica.

MODELO ATÓMICO DE BOHR
En 1913, Niels Bohr que trabajaba con Rutherford se encontraba buscando una explicación del porque el modelo atómico de Rutherford fallaba desde el punto de vista clásico, cuando leyó la teoría de Planck para la radiación del cuerpo negro.
El segundo postulado de Planck decía “ un oscilador solo emite energía cuando pasa de un estado de mayor energía a otro de menor energía” y consideraba la frecuencia de movimiento circular del electrón alrededor del núcleo análoga a la frecuencia del oscilador de Planck, por lo que se podría solucionar el problema.
El átomo solo emite radiación electromagnética cuando los electrones pasan de un nivel de mayor energía a uno de menor energía.
Entonces, basado en el modelo atómico de Rutherford, Bohr formuló para su modelo atómico del átomo de hidrogeno una serie de postulados.
- El átomo de hidrógeno se compone de un núcleo constituido por una carga +Ze y un electrón ligado a el por fuerzas electrostáticas.
- Existe un conjunto de estados energéticos (estados estacionarios) cuantizados en los que se mueve el electrón sin emitir radiación electromagnética. En ellos la energía es constante.

- Los electrones pueden saltar de un nivel electrónico a otro sin pasar por estados intermedios. Lo que implica la emisión o absorción de un único cuanto de luz (fotón) cuya energía corresponde a la diferencia de energía entre ambas órbitas. Si se absorbe la energía suficiente el electrón se libera(efecto fotoelectrico)
| ||||||||||||||||||||||||||||||||||||||||||||










No hay comentarios:
Publicar un comentario